열려있는 정책플랫폼 |
국가미래연구원은 폭 넓은 주제를 깊은 통찰력으로 다룹니다
※ 여기에 실린 글은 필자 개인의 의견이며 국가미래연구원(IFS)의 공식입장과는 차이가 있을 수 있습니다.
오태광의 바이오 산책 <30> 미완성 인간 유전체의 완전 해독( Closing on a complete human genome ) 본문듣기
작성시간
- 기사입력 2022년07월05일 16시45분
관련링크
본문
닐 암스트롱(Neil Aden Armstrong)이 1969년 우주선을 타고 달에 착륙하여 발자국을 남기면서 인류는 본격적으로 우주를 향하기 시작한 것과 같이, 인간 유전체가 해독된 2003년은 신비한 인간 생명 설계도 확보함과 더불어 그동안 인류가 완전히 해결하지 못한 난치 질병은 물론 노화(老化)의 비밀을 풀어 장수 할 수 있는 근거를 마련하였다.
또한, 개인 맞춤형 체계적인 건강 유지 방안을 확보하여 무병장수의 삶을 영위하면서도 삶의 질과 풍요로운 삶을 지속적으로 향상시킬 수 있는 인류 역사상 가장 놀라운 성과인 동시에 달에 인간 발자국을 남긴 것과 같은 놀라운 과학적 혁신과 진보를 달성하였다고 생각한다.
달에 지구인이 착륙하여 발자국을 남긴 미국의 아폴로 프로젝트에 대해 엄청난 돈을 투자하여, 단지, 달에 남긴 인간 발자국과 수집해 온 흙이 전부라고 혹평을 하면서 심지어 조작된 가짜라는 이야기조차 나돌 정도였다.
결론적으로, 인류가 우주로 향한다는 상징적이고 대단한 과학적 진보는 인정하지만, 짧은 시간 내 경제적 리턴(Return)이 없다는 것에 대한 허망한 마음이 그렇게 작용했을 것으로 판단한다.
그럼, 과연 “그렇게, 경제적 리턴은 없는 것 인가?”라는 질문에 “사실은 전혀 그렇지 않다.”라고 강조해서 대답할 수 있다. 경제적 리턴이 달에 착륙 후, 짧은 시간 내로 생각하면 실망이 될 수도 있지만, 달에 인간을 착륙하는 데는 엄청난 과학 기술적 진보가 있었고, 이런 획기적 기술의 응용은 시간이 지나면서 엄청난 경제적 효과를 가졌다. 즉, 초거대 과학기술 성과는 시간과 비용이 많이 투자되지만, 산업적 응용 시 보통 아주 큰 파급효과가 있어서 시간은 걸리겠지만 초거대 경제적 리턴이 가능하다는 것을 실증한 좋은 예이다.
아폴로 프로젝트 성공 후, 이루어진 대표적 몇 가지 초 경제적 리턴을 설명해 보자.
우선, 전기 통신 분야에서는 상업용 위성통신을 하는 COMSAT이 1962년 설립되었고, 요즘 흔히, 사용하고 있는 GPS도 완성되어, 이제 개인도 Navigator로 지구의 어떤 지역도 실시간을 검색할 수도 있을 뿐만 아니라 처음 가는 장소도 아주 쉽게 갈 수도 있고, 누구든지 언제든지 어디에서든지 이동통신(Mobile information)사용이 상호 연락이 가능하다. 이렇게 전기 통신 분야만 하더라도 엄청난 경제적 효과를 얻을 수 있었다.
또한, 아폴로 프로젝트 성공 후, 1980년대 개인용 컴퓨터(PC)가 개발이 시작하여 이제는 초등학생부터 회사원까지는 물론 거의 모든 사람이 컴퓨터를 사용하고 있다. 특히, 컴퓨터 과 모바일이 융합된 스마트폰(Smartphone)은 통신, 정보수집, 영업, 예술, 인문 등 모든 사회활동에 사용되어 대부분 사람의 생활필수품이 되었다.
에너지 분야도 연료전지와 태양 전지(Fuel cell/Solar cell)는 이미 전기자동차는 물론 태양광 발전 시대로 초거대 상용화 시대를 열었다. 그리고 현재의 위성정찰(LANSAT)로 기후, 광물 탐사, 환경관리까지 할 수 있게 되었고, 천문학 분야도 상상할 수 없는 멀고 먼 우주의 생성과 파괴를 연구하는 블랙홀(Black Hole)과 같은 시공간(時空間) 존재가 알려지면서 인간의 사고 능력을 무한히 넓힐 수 있었고, 파괴와 창조의 상반된 영역을 이해하면서 존재에 대한 철학적 영역도 무한하게 확장되었다.
현재, 개인의 우주여행이 이미 가시화되어 일반 지구인도 누구든지 우주인이 될 수 있고, 친환경 우주선, 우주 호텔 등을 위한 신건축기술, 우주농업, 우주 재활용 기술은 물론 지구에서와 마찬가지로 우주 환경산업 등 다양한 신규 산업이 우주로 공간으로 확장되고 있다. 우주 환경에서 얻어진 연구 결과는 극 초정밀물질 생산, 신 바이오 기술 개발, 우주 융합 산업 등 새로운 미래 산업이 창출되고 있어서 앞으로 다가올 제5차 산업혁명은 우주, 융합, 시공간 등이 기본이 될 것이다.
달 착륙을 위한 아폴로 계획은 당시 미국이 매년 GDP의 0.75%인 170억 US$를 사용하였고, 달 착륙까지는 약 1,940억 US$(약 230조 원)란 엄청난 비용을 사용하였지만, 전술한 몇 가지 산업적 응용 기술로 얻어지는 실물 경제적 가치에 비하면 아폴로 프로젝트의 비용은 ‘빙산의 일각’이라고 개인적으로 추정한다. 사실은 겨우, 1,940억 US$로 셀 수 없이 많은 분야에 이미 엄청난 경제적 보답을 받았다고 말할 수 있고, 미래의 경제적 파급 가치는 더욱 커질 것으로 생각한다.
아폴로 프로젝트와 비슷하게 시작된 초대형 과제인 인간 유전체 해독과제도 바이오산업뿐만 아니라, 의 약학, 식품, 농수산, 화학, 건설, 의류, 환경 등 다양한 산업에 엄청난 기술적 혁신은 물론이고, 새로 생기는 수 없이 많은 신규 산업과 일자리는 무한한 산업적 가치를 창출하고 있다. 무엇보다 중요한 것은 개인 유전체 기반의 개인의학(Personal medicine)이 등장하여 유전체중심의 예방/치료, 생산성 확대, 빅데이타와 인공지능, 뇌신경공학, 유전체 편집등 완전히 새로운 산업 생태계가 정립되고 있다.
의학 분야는 진단과 치료 분야에 획기적 발전을 가져와서, 정밀의학(Precision medicine)이 자리 잡으면서 사회 전반이 유전체(Genome to Society)에 영향을 받아서 질병 치료(Illness)에서 종국에는 예방을 통한 복지(Wellness)사회 구현으로 근본적인 혁신이 이루어지고 있다.
이런 기술/사회적 변화는 개인의 개성(Privacy), 개인 식별 (Discrimination), 지적 재산권(Patent), 보험(Insurability), 고용(Empolyability), 문화적 및 법적 수용등 거의 모든 인간 생활 분야에 영향을 미쳐서 신산업 창출 및 신고용 분야는 물론, 인문, 법학, 경제 등 모든 사회분야에서도 큰 변화를 가져왔다.
인간 유전체 초기해독은 2003년에 13년간 아폴로 프로젝트의 약 1/50인 38억 US$의 비용을 사용하여 백인을 대상으로 분석을 완료했지만, 초기 유전체 해독은 완벽하게 인간유전체를 해독한 것은 아니었다. 2003년 인간유전체 해독 후, 기술적으로 어려워 해독하지 못했던 유전체 부위를 꾸준히 보완하여 왔다. 우리나라도 2016년에 해독하기 어려운 190개의 공백이 있는 미완의 유전체를 해독하여, 105개를 완벽하게 해독하여 보고하였다.
하지만, 여전히 기술적 한계로, 72군데는 해독할 수 없어서, 결국, 인간유전체 염기서열의 8%는 전혀 해독하지 못하고 있었다. 하지만, 처음 인간유전체 해독을 발표한 2003년부터 약 20년이 지난 2022년 3월에 인간유전체 염기서열과 정보해석을 100% 성공하였다고 과학전문지 ‘Science’는 발표하였다. 이번 글에서는 인간 유전체 해독과정을 순서대로 설명하기 위해서 인간유전체가 포함된 23개의 염색체에서부터 완전히 인간유전체가 해독되는 과정을 설명해 보고자 한다.
<염색체>
인간 유전체는 23개의 염색체(Chromosome)로 구성되어 있는데, 우리는 부모(父母)로부터 각각의 염색체(n)를 받아서 상동염색체(2n=어머니(n)+아버지(n))로 구성하여 결국 사람은 46개의 염색체를 가지고 있는 셈이다. 인간염색체는 남녀 체세포에 공통으로 들어있는 22개의 상염색체(常染色體, Autosomal chromosome)로 이루어진 상동염색체 (相同染色體, Homologous chromosome)로 되어 있다. 남녀 성별에 따라 다르게 가지고 있는 성염색체(性染色體, Sex chromosome)는 X염색체와 Y염색체가 있는데, 남성의 경우는 XY, 여성의 경우는 XX 염색체로 되어있어 결국 남성은 22(2n=44)개의 상염색체에 XY(2n=2)로 구성된 성염색체를 더하여 23(2n=46)개의 염색체로 구성되어있고, 여성도 역시 22개(2n=44) 상염색체에 성염색체인 XX(2n=2)가 포함되어 모두 23(2n=46)개의 염색체를 가진다.
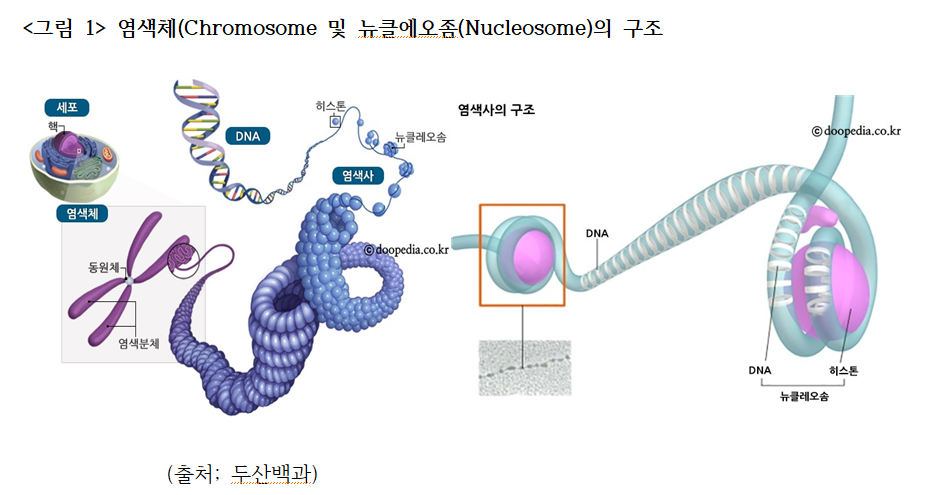
염색체는 핵 속에서 아주 굵은 실타래가 감긴 모양을 구조물<그림 1>로 존재하는데, 염색사(絲)는 DNA와 히스톤(Histone)이라는 단백질을 감아서 만든 구슬 모양의 뉴클레오좀(Nucleosome)이 길게 연결되면서 촘촘하게 응축되어 마치 큰 실타래가 굵게 다시 감겨있어서 마치 커다란 ”X“자 모양의 염색체를 형성한다.
인간 DNA의 총 길이는 약 2m나 되는데, 지름이 5㎛(10-6m)밖에 되지 않는 아주 작은 핵 속에서 보관하는 방법은 이렇게 굵은 실타래 모양으로 고도로 응축하여 만들어 염색체로 보관하고 있다. 인체 세포의 크기는 대략 100㎛이고, 세포 속에 핵(Nucleus)이 있고 핵 속에 염색체가 존재한다.
염색체를 해부<그림 1>하면 DNA로 연결된 염색사가 히스톤이란 단백질을 감고 있는 구슬 모양의 뉴클레오좀이 길게 연결되어 전자 현미경으로 보면 실에 엮은 구슬(Bead-on-String)과 비슷한 모양을 하고 있다. 히스톤을 완전히 떼어내고 DNA만으로 구성된 염색사의 DNA는 4개의 염기인 A,T,C,G가 한 개씩 길게 연결된 염기의 서열(序列)을 결정하는 것이 유전체의 염기서열 해독이다. 해독된 유전체의 서열은 무질서하게 A,T,C,G로 아주 길게 연결되어 30억 이상의 염기서열로 이루어져 있어서 마치 간첩들이 사용하는 문서처럼 남이 읽을 수 없게 암호화(暗號化)되어 있다.
암호를 해독하기 위해서 난수표(亂數表)가 필요하듯이 20개의 아미노산을 나타내는 암호화된 3개의 염기서열과 단백질이 시작되는 위치(AUG)와 끝나는 위치(UAA, UAG, UGA)를 나타내는 마치 난수표와 같은 코돈(Codon)을 이미 알고 있어서 길게 읽힌 인간 유전체 염기서열을 아미노산으로 이어진 단백질의 서열로 바꿀 수 있었다. 아미노산 서열을 알고 있는 단백질은 이미 아미노산 서열이 알려진 단백질과 상동성(相同性)을 비교함으로 단백질 기능을 분석할 수 있다. 길게 연결된 DNA 염기서열이 히스톤이란 단백질을 감고 있는데, 초기에는 히스톤이 DNA를 감는 실패처럼 단순한 단백질이라고 생각했는데, 점차 연구를 통해서 실패의 역할뿐만 아니라 중요한 생체 기능을 하는 것이 알려졌다.
뉴클레오좀의 중심을 이루는 히스톤 단백질에는 다양한 길이의 N-말단의 꼬리를 가지고 있다는 것을 밝혔다. DNA가닥 사이는 H2B, H3의 N-말단의 꼬리가 있고, DNA가닥 상하에는 H2A, H4의 N-말단의 꼬리가 있다. 각 히스톤 N-말단의 꼬리에 포함된 아미노산인 라이신(Lysine), 세린(Serine) 알지닌(Arginine)위치를 생체 내에서 아세틸화 (Acetylation), 메틸화(Metylation)등과 같은 화학반응이 일어나면 유전자에서 유전정보를 mRNA로 옮기는 전사(Transcription)가 촉진, 억제, 신장과 관련된 중요한 역할을 하는 것을 밝혀졌다. 전사가 촉진되면 단백질이 빨리 만들어지면서 생체반응이 빨라질 것이고 억제하면 생체반응이 일어나지 않게 되어 생체조절에 매우 중요한 역할을 한다.
염색체 수는 사람이 46개인데 비해 보통 모기는 6개, 말은 66개, 영장류는 48개, 고사리는 92개, 섬모충류는 3,000만 개나 있다고 하니 염색체 수의 많고 적음과 고등생물의 여부나 지능과는 무관하다고 밝혀지고 있고, 이 분야에 대해서도 더 큰 노력을 한다면 각기 다른 생물의 살아가는 기본원리를 이해할 수 있을 것이다.
<인간 유전체의 2003년 해독>
인간유전체 해독은 1984년 미국 정부에서 제안되었고 초기에는 워낙 큰 프로젝트이고 당시의 과학기술로는 해독/분석 자체가 어려워서 단지 기술 가능성과 타당성을 검토하였고, 1990년부터 미국 국립보건원(National Institute of Health, NIH)이 중심이 되어 인간유전체 해독이 시작되었다. 1993년 영국 Sanger center가 합류하였고 이어서 독일, 중국, 프랑스, 일본이 참여하여 최종 6개국의 공동 노력과 셀레라 지노믹스(Celera Genomics)라는 민간 법인의 후원을 받아서 인간 유전체 해독이 이루어지게 되었다. 결국, 다국적의 거대한 Consortium이 형성되어서 연구가 활성화되면서 13년이 걸려서 일부 기술적으로 어려운 점을 남기고 2003년 인간 유전체 해독을 완성하였다.
인간 유전체 해독을 하면서도 많은 난관이 있었다. 초기의 인간유전체 해독은 생어(Sanger) 염기서열 결정 방법을 바탕으로 사업이 진행되었다. 하지만 이 방법은 한 번에 읽을 수 있는 서열의 길이가 불과 200~300개 정도에 불과하여, 현실적으로 중복된 DNA 절편 없기 때문에 연속해서 읽어 나가는 것은 불가능하였다. 끊김 없이 연속된 서열로 읽어내기 위해서는 DNA 절편의 중첩 부위 정보를 이용해야 하는데, 크게 다음 두 가지 전략이 사용되었다.
제임스 왓슨(James Dewey Watson, 1928~ )이 이끄는 국제 협력 연구팀의 전략은 클론-컨티그(Clone-contig)방법으로 전체 서열을 순서를 정해서 서열을 차근차근 분석하여 전체적인 조각을 맞추어 나가는 것이었다. 이 방법은 매우 느리게 진행되었지만 대신에 유전체의 50% 이상을 차지하고 있는 반복서열로 인한 서열들의 엉킴은 많이 줄일 수 있는 장점이 있었다. 속도가 너무 느려서 시간이 아주 많이 걸리는 단점이 있다.
제임스 왓슨의 고전적으로 전체 인간 유전체를 순서대로 잘라서 한 개씩 한 개씩 붙여나가는 지루한 방식에 반대한 크레이그 벤터(Craig Venter, 1946- ) 팀은 무작위로 유전체를 잘라내서 마치 장남감 “레고(LEGO)”를 맞추듯이 조립하는 전혀 다른 전략으로 인간유전체 과제를 완성하려고 하였다.
사실 제임스 왓슨과 크레이그 벤터는 초기 NIH에서 인간유전체 해독과제를 같이하였지만, 연구방식에 대한 크레이그 벤터가 제임스 왓슨과의 불화를 야기하여 NIH를 그만두고 나와, 셀레라 지노믹스(Celera Genomics)라는 회사를 세워 인간 유전체 사업에 뛰어들게 된다. 즉, 제임스 왓슨의 순차적 분석과는 다르게 크레이그 벤터는 유전체 DNA를 무작위로 작게 자른 단편들을 8~10배로 빠르게 읽어낸 후, 이들 조각 정보들이 가지고 있는 겹침 서열 정보를 컴퓨터 알고리즘으로 연결하는 작업(Sequence assembly)을 성공시킴으로써, 속칭 전체 유전체 산탄총(Whole-genome shotgun sequencing)방법을 개발하여 인간 유전체 서열분석이 가능함을 증명하였다.
결국 크레이그 벤터는 무작위적인 시퀸싱을 통해 얻어낸 무작위 유전체 서열 단편들을 발현서열 꼬리표(expressed sequence tag, EST)를 이용하여, 세포별 유전체에서 발현되는 코딩 부위의 차이를 빠르게 조사하는 방법을 제안하여 전 세계적으로 논쟁과 주목을 동시에 받았었다. 크레이그 벤터는 더 나아가 인간 유전체 서열도 전체 게놈 산탄총(whole genome shotgun)이라는 방법으로 훨씬 더 빨리 알아낼 수 있다고 공언하여 국제 협력 연구팀을 긴장시켰다. 이 방법은 확실히 빨랐지만, 인간 유전체 전체에 걸쳐 있는 반복서열 때문에 부정확한 서열 연결이 많이 발생할 수밖에 없는 단점이 있었다.
결국, 국제 협력 연구팀과 크레이그 벤터 팀은 서로의 방법론들을 보충적으로 사용, 보완하여 2001년 초안(Draft)을 함께 발표하였고, 2003년 거의 완성된 인간 유전체를 공표할 수 있었다. 2001년 끝난 후 유전자 지도의 초안이 발표되면서 기능이 있는 단백질 유전자 수는 약 25,000개 정도로 예상되었으나, 2013년 공개된 인간 유전체 염기 정보에 관한 최신판인 GRCh38에 의하면 사람의 기능 유전자 수는 최종적으로 19,950개로 발표되었다.
<인간유전체 해독보완 및 완성(2022년)>
2003년 발표된 인간 유전체 해독은 당시 과학기술로 해독할 수 있는 유전체 영역만을 분석한 결과를 발표하였다. 2003년 인간 유전체가 발표된 후, 많은 과학자의 노력에도 불구하고 도저히, 기술적 한계로 해독할 수 없는 염기서열이 여전히 남아서 완벽한 유전체 해독은 할 수 없었다. 한국인 인간유전체는 2009년 서정선(서울대학교) 교수와 박종화(울산과기대) 교수가 각각 따로 한국인 인간유전체를 분석하여 발표하였다. 2016년까지는 인간 유전체 중 해독이 어려운 190개의 공백 있었는데, 서정선 박사(마크로젠)의 노력으로 105군데를 완벽하게 해독은 했지만, 여전히 72군데는 93%까지만 해독할 수 있어서 결국 기술적 한계는 극복할 수 없었다.
최종적으로 해독하지 못하는 일부 염기서열이 8%를 남기게 되어서 여전히 완벽한 유전체 해독은 하지 못했다. 마지막까지 유전체 해독이 어려웠던 부분은 염색체 끝부분 텔로미어(Telomer, 末端小粒)부분이고 다른 염색체의 텔레미어 까지는 길고 반복되는 염기서열이 아주 많아서 결국 분석하지 못했다. 텔로미어는 세포의 수명을 결정짓는 역할을 하는 세포의 시계의 역할을 하는 DNA이다. 세포가 분열이 일어나면 염색체와 DNA를 복제(複製)하는 효소는 염색체 끝에 있는 텔로미어는 복제를 계속할 수 없어서 유전체 해독에 기술적 문제점이 되었다.
미국 인간게놈연구소(NHGRI)와 캘리포니아 주립 산타쿠르즈대학 등 세계적으로 구성된 텔로미어 투 텔로미어(Telomer to Telomer, T2T) Consortium이 3년간의 노력으로 2022년 3월 드디어 유전체의 빈틈을 완전히 채워서 인간유전체 정보해석을 완료하였다. T2T 유전체 해독으로 인간의 삶에 필수적인 단백질 99개의 신규유전자와 아직은 기능이 불분명한 2,000개의 단백질 유전자를 새로 발견하였다. 염색체 끝부분은 길게 반복되는 텔로미어와 세포를 나누는 센트로미어 (Centromere) 가 있어서 해석이 어려웠는데 나노포아 시퀀싱 (Nanopore sequencing)이란 첨단 신기술이 개발되어서 100% 해독을 가능하게 하였다.

지금까지 텔로미어와 센트로미어는 어떤 단백질도 생산할 수 없는 염기로 코딩되어 있어서 결국 단백질을 만들지 못하기 때문에 생명 활동에 도움이 되지 않는다고 하여 쓰레기 DNA (Junk DNA)라고 간주하였다. 하지만, 노화가 진행되면 텔로미어가 짧아진다는 현상은 이미 알고 있지만, 중요한 세포 기능이 새로 밝혀져서 텔로미어가 잘못될 시, 암의 원인이 된다고 한다. 또한, 센트로미어는 세포분열 시 DNA가 2배가 되면서 X자형의 실타래의 가운데 중심에 있고, 센트로미어 중심에서 떨어져 있을수록 열성의 과거의 유전자 서열이 나타나서 먼 조상인 유인원부터 물려받은 센트로미어까지 존재하고 있어서 마치 유전자 안에 있는 화석(化石)으로 비유할 수 있다.
우리가 생물의 화석에서 과거의 중요한 경험과 미래를 예측할 수 있듯이 텔로미어와 센트로미어 부분을 잘 해석하면 유전자의 작동원리, 유전병, 인간 다양성과 진화 등을 이해하고 현존 인류가 문제시하고 있는 난제(難題)를 해결하는 데 중요한 역할을 할 것으로 기대할 수 있다.
아무튼 33년이란 오랜 연구과정을 거쳐서 인간 유전체를 100% 완벽히 해독하여 인간 유전체의 크기는 지금까지 30억 염기쌍으로 알고 있었는데, 이제는 정확히 32억 염기쌍으로 2억 염기쌍이 추가로 해독되었고, 단백질은 지금까지 약 2만 개로 추정하였는데, 이제 2만 2천 개로 확정하였다. 이번 인간유전체의 추가된 획기적 발견은 2022년 3월에 과학학술지 Science에 6편의 논문을 출판하고 “Science지”의 표지<그림 2>로 선정되었고, 극도로 긴 염기서열을 읽어내는 신규 첨단 유전체 해석기술은 Nature methods에 실렸다.
<맺는말>
인간유전체는 2003년 완성되었다고 발표할 때 많은 사람은 완벽하게 해독되어 이제는 인간유전체로 무엇이든 할 수 있다고 생각했을 것이다. 그럼 우린 2003년에 해독된 30억 염기쌍과 약 2만 개의 코딩된 단백질을 완벽하게 활용하고 있는가? 그렇지는 않다, 여전히 기능을 알 수 없는 것이 많고, 한 개의 단백질이 가진 중복된 여러 기능은 물론, 단백질 기능 간 복잡한 Network와 조절기능은 아직도 갈 길은 멀다. 전체 인간유전체 중 단백질을 나타내는 염기서열 정보는 불과 약 2% 정도이고 아직 기능이 모르는 98%인데 기능단백질을 암호화(Coding DNA)하지 않는 98% 비 암호화 서열(Non-Coding DNA)은 기능과 용도가 없어서 유전체분석 초기는 생명 활동에 도움이 되지 않는다는 이유로 쓰레기 DNA (Junk DNA)라고 비하하였다.
염기서열의 변화 없이 어떤 형질이 후손에게 전달되는 후생 유전학적 유전(Epigenetc inheritance) 등이 새로운 사실로 밝혀짐에 따라서 현재로는 전혀 기능이 없다던 쓰레기 유전자의 중요한 기능이 점차 밝혀지면서 활성화되다가 드디어 이번 유전체 완성분석으로 세포 기능에 중요한 역할 한다는 것이 새로 밝혀졌다. 쓰레기로 여긴 Junk DNA가 잘못되면, 암의 원인이 된다는 중요 결과와 유전자 작동원리와 유전병, 인간 다양성과 진화 등을 이해하는 데 중요한 역할을 할 것으로 기대하여 쓰레기가 아닌 황금을 캐내는 느낌이 든다. 한 가지 주의하여 보아야 할 사실은 NIH에서 인간 유전체를 해독할 시, 서로 다른 연구 방법에 대해서 불화는 있었지만 결국 힘을 합쳐서 2003년 인간유전체 해독을 발표할 수 있었다. 새로운 과제를 할 때 과제의 중첩 문제로 대부분 한 개 우월한 과제만 지원하는데, 정말로 중요한 과제는 중첩을 배제하는 것이 아니라 함께 연구하거나 아예 의도적 중첩으로 최종적으로 협업하는 시스템 구축이 매우 중요하다.
이번에 인간 유전체 완벽한 해독은 과학자들이 T2T Consortium으로 연합하여 연구하였기 때문에 가능하여, 인류 전체 문제를 해결하는데 는 연구 협업의 중요성을 부각시켰다. 앞으로 일어날 수도 있는 인류 생존에 큰 영향 주는 이번에 코로나19같은 감염 병 연구에는 국적 없는 연구협업이 중요하다. 특히, T2T Consortium 연구팀은 유전체분석을 넘어 많은 사람의 유전체 정보 분석을 위해 “인간 판 제 놈 레퍼런스 컨소시움(Human Pan-genome Reference Consortium)”을 구축하여 협업한다니까 기대되는 바가 크다.
- 기사입력 2022년07월05일 16시45분
- 검색어 태그 1
댓글목록
등록된 댓글이 없습니다.
